注冊證號 國藥準(zhǔn)字SJ20210003
上市許可持有人英文名稱 Kyowa Kirin Co., Ltd.
上市許可持有人地址(英文) 1-9-2 Otemachi, Chiyoda-ku, Tokyo, Japan
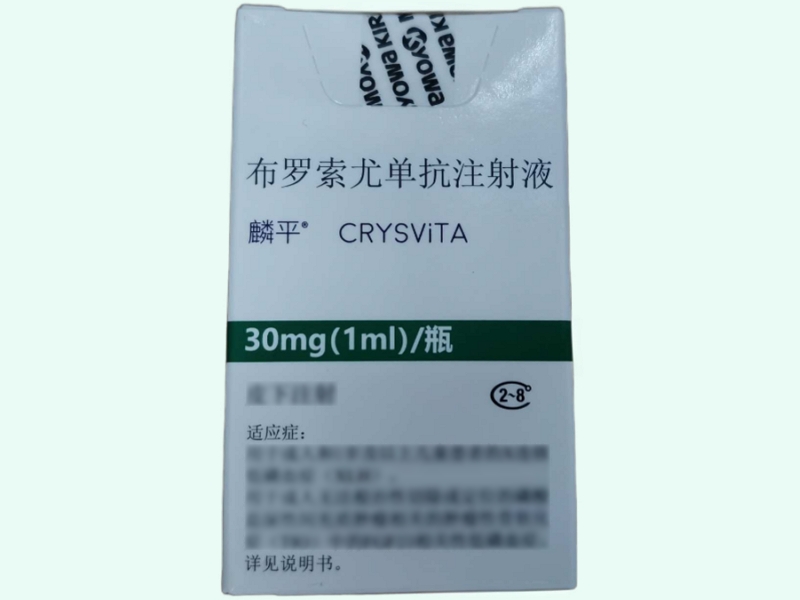
產(chǎn)品名稱(中文) 布羅索尤單抗注射液
產(chǎn)品名稱(英文) Burosumab Injection
商品名(中文) 麟平
商品名(英文) Crysvita
劑型(中文) 注射劑
規(guī)格(中文) 西林瓶裝:30mg(1ml)/瓶
包裝規(guī)格(中文) 1瓶/盒
生產(chǎn)廠商(英文) Kyowa Kirin Co., Ltd., Takasaki Plant
廠商地址(英文) 100-1 Hagiwara-Machi, Takasaki-Shi, Gunma, Japan
廠商國家/地區(qū)(中文) 日本
廠商國家/地區(qū)(英文) Japan
發(fā)證日期 2021-01-05
有效期截止日 2026-01-04
境內(nèi)責(zé)任人名稱 協(xié)和麒麟(中國)制藥有限公司
境內(nèi)責(zé)任人統(tǒng)一社會信用代碼 91310000607373815W
境內(nèi)責(zé)任人通訊地址 中國(上海)自由貿(mào)易試驗(yàn)區(qū)龍東大道970號
藥品本位碼 86982988000039
產(chǎn)品類別 生物制品

